糖类分析,用氨基柱还是糖柱?
糖类作为生物体重要的能量来源和代谢中间产物,一直备受关注。近年来,随着科技的不断进步,糖类研究迎来了前所未有的发展机遇,研究深度和广度均实现了显著飞跃。
糖类是由碳、氢、氧三种元素组成的有机化合物,通常以多羟基醛、酮及其衍生物的形式广泛存在于自然界。根据组成和结构的不同,糖类可分为单糖、低聚糖和多糖。
单糖:是最简单的糖类,如葡萄糖、果糖等。
低聚糖:是由2-10个单糖分子脱水缩合而成的小分子化合物,如麦芽糖、蔗糖等。
多糖:是由许多单糖分子脱水缩合而成的高分子化合物,如淀粉、纤维素等。

进入21世纪,糖类研究已经涉及到多个领域,包括生命科学、材料科学、能源科学等。随着生命科学的发展,糖类与生物大分子的相互作用逐渐成为研究热点。例如,糖类在蛋白质、核酸等生物大分子的合成和修饰过程中发挥重要作用。此外,糖类还参与了细胞识别、信号转导、免疫应答等生命活动。
糖类分析主要分两类。
第一类:单糖、双糖、寡糖的分离。
第二类:多糖的分子量及其分布。
糖类物质的分析,通常在液相色谱中使用氨基柱。但随着色谱技术的发展,分析糖类的色谱柱也越来越多,目前苯乙烯-二乙烯基苯共聚物为基质的磺化柱,也成为糖类测试的主流,其中聚合物磺化色谱柱又分为磺化氢型(如SUGAR-H)、磺化钙型(如SUGAR-Ca)、磺化钠型等等。那么如此众多的糖分析柱,应该如何选择呢?

氨基柱和糖柱优缺点
1. 检测器要求:检测糖类分子时,检测器一般为示差检测器,这类检测器对样品浓度有一定要求,因此样品需要有较高的浓度以保证检测的灵敏度。
2. 流动相的区别:糖柱的流动相为纯水或硫酸水溶液,糖类分子的溶解一般不是问题,而使用氨基柱分离时,其流动相一般为70:30的乙腈水。当样品中含糖种类多或含量较高时,用70:30的乙腈水定容样品,可能会由于溶剂与样品间的溶解度差异导致样品析出,影响分离效果和检测结果的准确性。
那是否能用纯水定容呢?不建议,因为可能会有溶剂效应,导致峰形异常。另外,从溶剂的经济性和环保性上比较,糖柱的成本更低,对环境的潜在污染少,相较于使用有机溶剂如乙腈的氨基柱系统,更为经济环保。
3. 仪器配置方面:糖柱需要70℃以上高温,而部分液相的柱温箱可能无法达到,因此在设备成本上,使用糖柱的要求要高于氨基柱。
4. 柱子寿命方面:氨基键合相在酸性条件下易流失,碱性条件下硅胶容易被破坏,在分析葡萄糖、果糖、麦芽糖、乳糖这些还原性糖时,糖上的醛基还会与氨基发生反应,使氨基掉落或变性,大大减短了氨基色谱柱使用寿命。
糖柱为苯乙烯-二乙烯基苯共聚物为基质,交联度低,相比硅胶基质而言,机械强度较差,在柱温升到设定值之前流速需稳定在0.2-0.3mL/min,太大的应力会破坏柱床,流速增减量也要以0.1mL/min为单位,稍不小心可能会导致色谱柱报废。
5. 分离机理的区别:糖柱的分离模式主要为配位交换模式。配位交换是利用糖类分子上的羟基与柱相上金属离子形成络合物的相互作用(即配位交换能)的分离模式。根据不同糖的羟基个数不同、空间结构不同,他们的配位交换能不同,因此能起到分离的作用。
配位交换能也会根据离子种类不同而不同,市面上现有Ag+柱、Li+柱、Na+柱、Zn2+柱、Ca2+柱、Ba2+柱、Pb2+柱,对离子形成的络合力依次由弱到强;而氨基柱主要官能团是丙胺基,主要是通过亲水作用起到分离的效果。
因此氨基柱的优势在于同时分离含有单糖、二糖、三糖等不同聚合度糖的样品;糖柱则更适合分离单糖、有机酸和糖醇,如果聚合度>4,分离度效果可能会变差。

由图1可以看出氨基柱在分离单糖和单糖、或者双糖和双糖时难度较大,但是单糖和双糖之间分离效果较好。
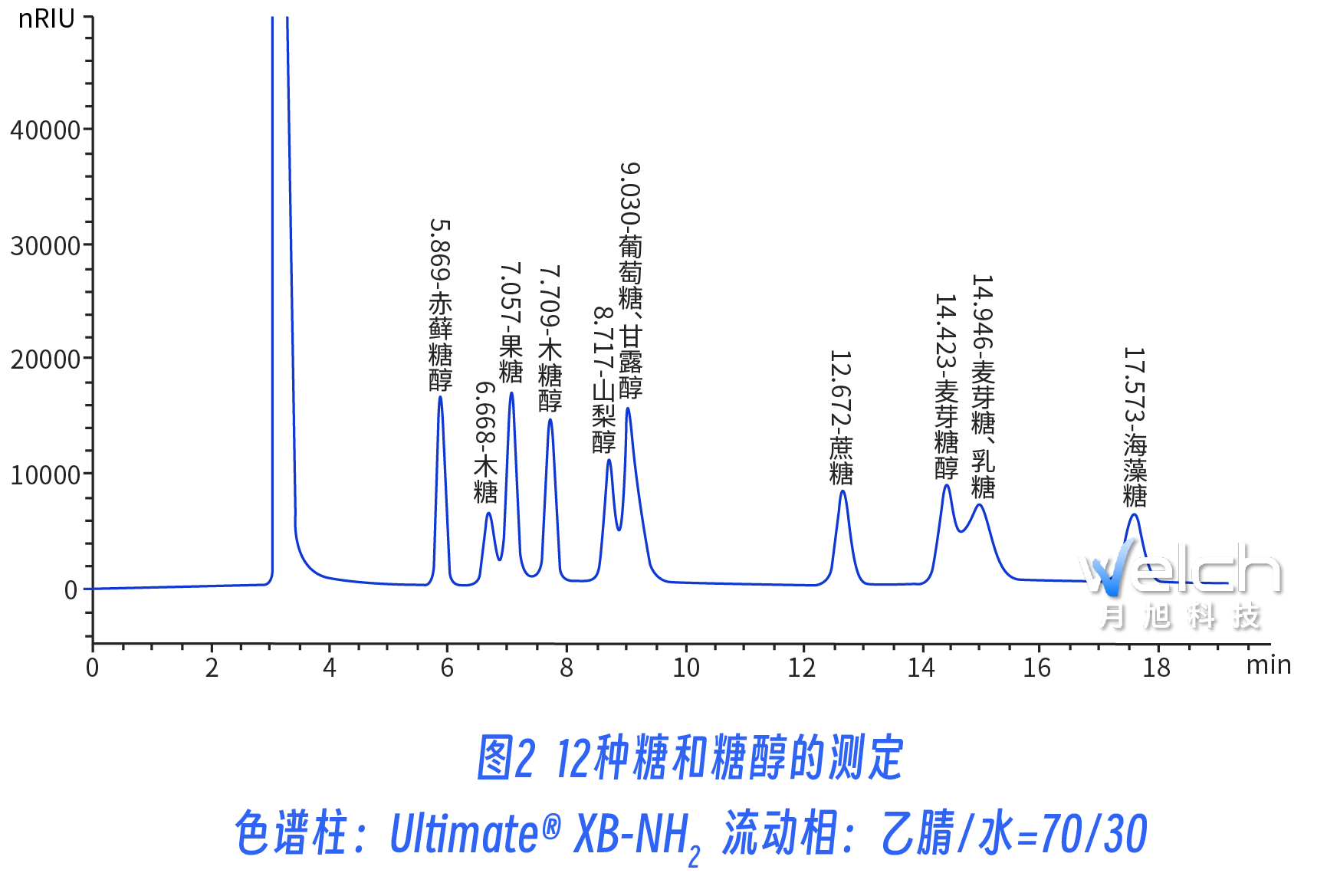
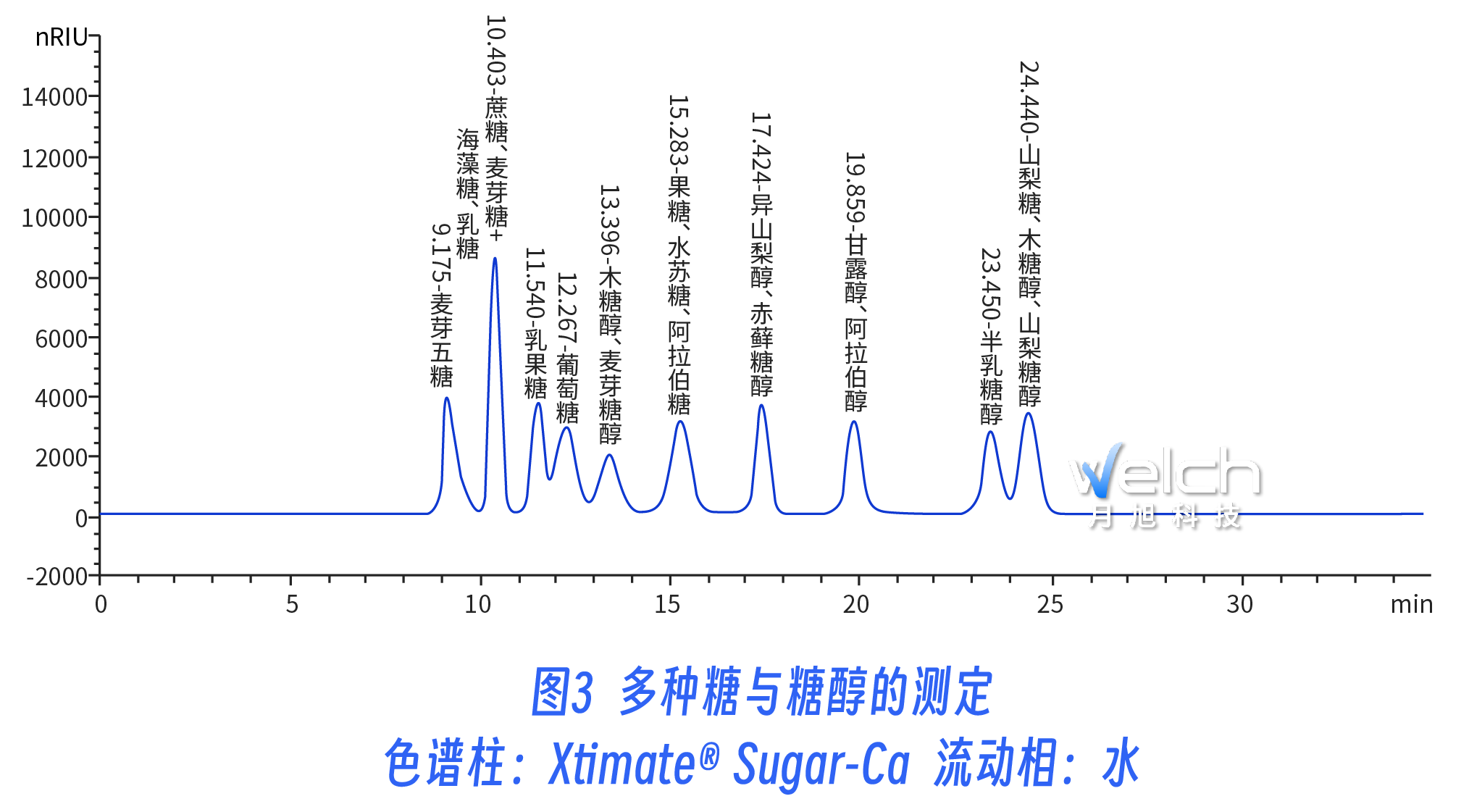
由图2和图3可以看出,钙型糖柱和氨基柱在分离糖和糖醇时分离效果是不同的。氨基柱对糖醇和糖的分离较难,而在钙柱上糖醇出峰时间要长于糖的出峰时间(比如麦芽糖和麦芽糖醇在氨基柱上分离度较差,在钙柱上能完全分离),所以在分离糖醇和糖时建议优先考虑糖柱;另外根据报道,随着糖的聚合度的增加,因为体积排阻的原因,会导致在钙柱中保留降低,分离度下降。
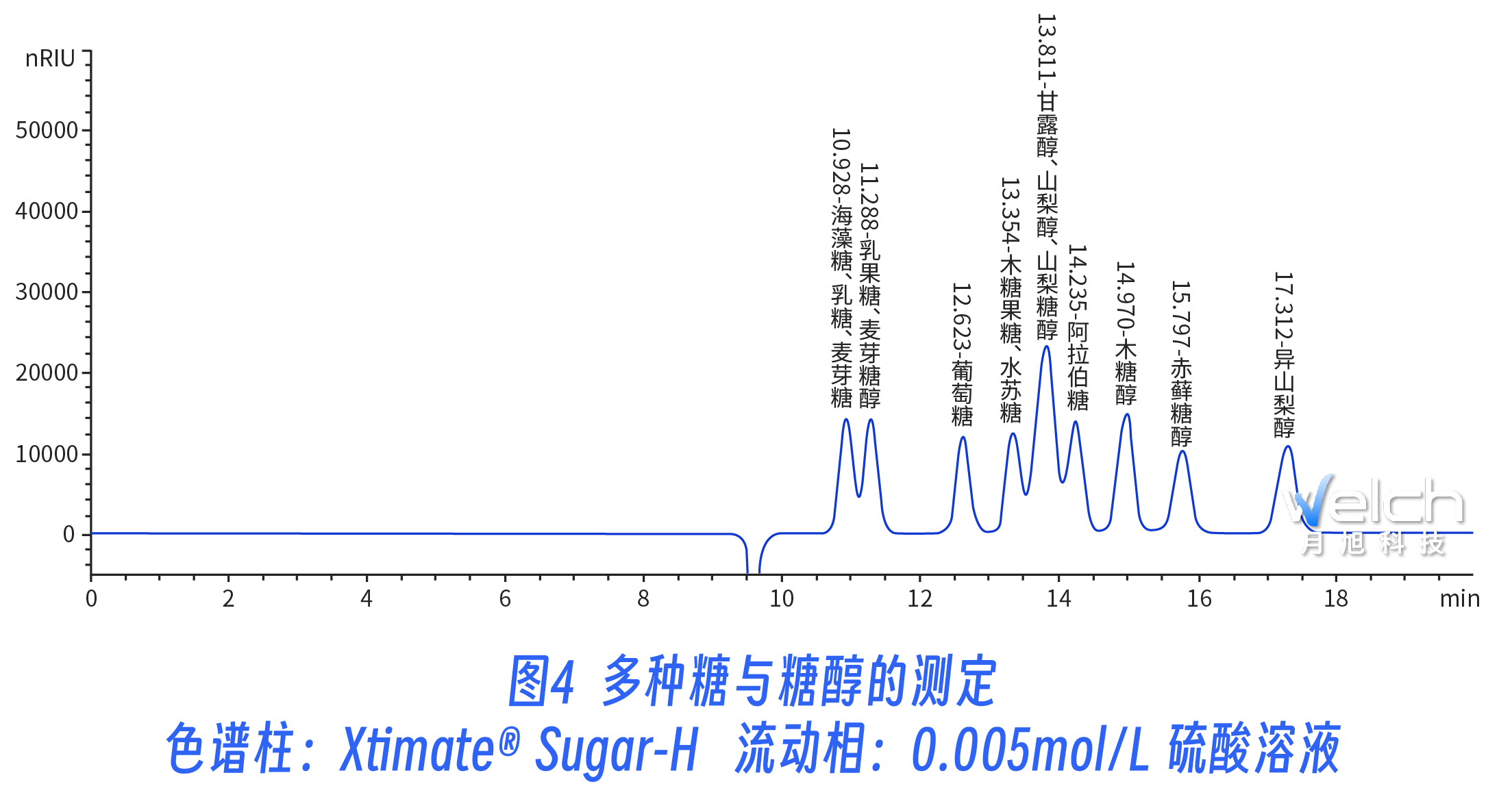
Sugar-H柱和Sugar-Ca柱在分离糖与糖醇时有不同的选择性,且多数情况下,Sugar-H被用来分离多种有机酸。Sugar-H中磺基官能团对某些糖类(比如蔗糖和绵子糖)起分解催化作用,温度越高分解越快,建议使用时温度<40℃。

